Catharine Layton and Andrew J. Aubin Waters Corporation, Milford, MA, US
A medida que avanza la legalización del cannabis para uso medicinal y recreativo, se desea disponer de métodos analíticos sencillos y fiables para la separación y f. Aquí se presenta la modificación de una separación isocrática por HPLC de 16 cannabinoides a una separación en condiciones UPLC. La conversión del método aumenta más de 2 veces en la productividad de las pruebas, manteniendo la linealidad, la selectividad y la idoneidad observadas en la separación HPLC.
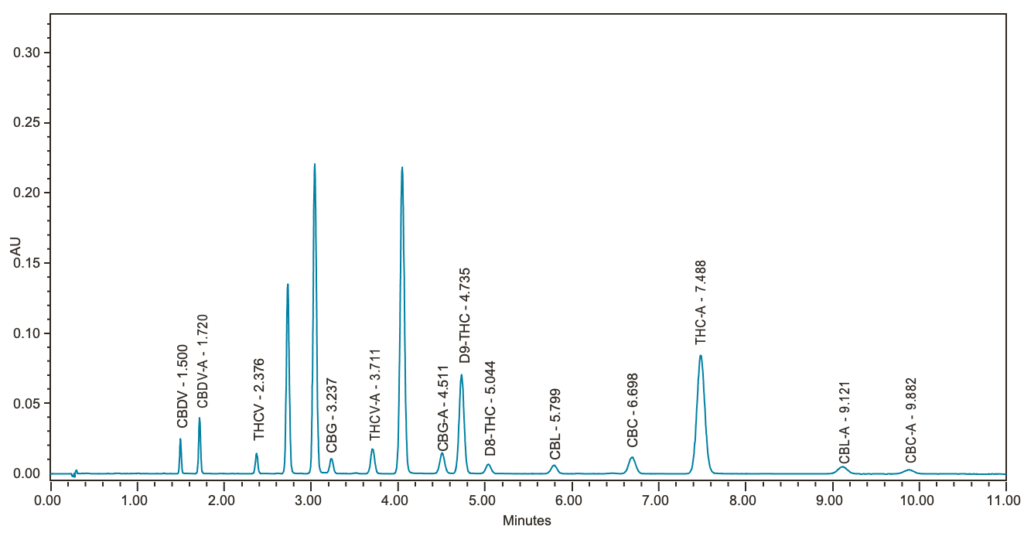
0,161 mg/mL) por UPLC. Todos los demás cannabinoides a 0,016 mg/mL, inyección de 0,7 µL, detección a 228 nm.
| CONDICIONES EXPERIMENTALES | |
| Sistema de LC: | ACQUITY UPLC Clase H |
| Columna: | CORTECS UPLC Shield RP18, 90 Å, 1,6 µm, 2,1 × 100 mm |
| Caudal analítico: | 0,7 mL/min |
| Fase móvil A: Agua con 0,1% de TFA Fase móvil B: Acetonitrilo | Isocrática: 41:59 fase móvil A/fase móvil B |
| Detector: | ACQUITY UPLC PDA (longitud de onda: 228 nm a 4,8 nm de resolución) |
| Volumen de inyección: | 0,7 µL para 1,0 mg/mL de referencia |
| Temperatura del horno | 35 °C |
| Software: | Empower 3 CDS |
La columna de HPLC, el caudal y el volumen de inyección descritos en la nota de aplicación se ajustó a los parámetros del método de UPLC como se describe en el capítulo general de la USP <621> titulado “System Suitability” para las separaciones cromatográficas isocráticas. La relación L/dp del método de HPLC (donde L es la longitud de la columna ydp es el diámetro de las partículas) se conservó en la medida de lo posible manteniendo la química de partículas CORTECS Shield RP18, 90 Å y pasando de una columna de 2,7 µm 4,6 mm × 150 mm a una columna CORTECS UPLC de 1,6 µm con 2,1 mm × 100 mm. El volumen de inyección se escaló proporcionalmente para tener en cuenta la longitud y el diámetro de la columna de acuerdo con la ecuación de escalado geométrico.
Preparación de las curvas estándar: La linealidad de los cannabinoides primarios (-)Δ9-THC y CBD se determinó para 10 concentraciones entre 0,004 mg/mL y 1,000 mg/mL, preparadas mediante dilución en serie en metanol utilizando los estándares exentos de DEA como demostración representativa de la linealidad del método. Muestras: Se obtuvieron cuatro muestras representativas de flores y concentrados de cannabinoides preparados de un laboratorio local de pruebas en Massachusetts y una muestra adquirida de un laboratorio de procesamiento de cáñamo en Vermont. Las muestras fueron preparadas por los fabricantes de la siguiente manera: Para la flor, se añadió una porción de material vegetal homogeneizado a acetonitrilo o etanol y se sonicó durante 20 minutos. El extracto subsiguiente se filtró a través de un filtro de punta de jeringa de 0,22 µm directamente en un vial de muestra de 2 mL para su análisis. Los concentrados se prepararon de forma similar con isopropanol como disolvente de extracción.
RESULTADOS Y DISCUSIÓN
En el método presentado, se utilizan condiciones de UPLC para separar 16 cannabinoides en 10,5 minutos utilizando ácido trifluoroacético (TFA) al 0,1% en una mezcla de agua y acetonitrilo, en condiciones isocráticas, combinadas con una columna CORTECS UPLC Shield RP18 y el sistema ACQUITY UPLC H-Class (Figura 1). La selectividad observada en condiciones de HPLC se mantuvo en la separación por UPLC,
y la resolución (Rs) de los 16 compuestos fue >2,0 (Tabla 3, Figura 2), lo que cumple con las recomendaciones de Rs para una cuantificación fiable.Las curvas de calibración multipunto para dos cannabinoides representativos (CBD y (-) Δ9 -THC) demostraron una buena linealidad en R2 >0.9998. La curva de calibración para el CBD se presenta en la figura 3, como representante.
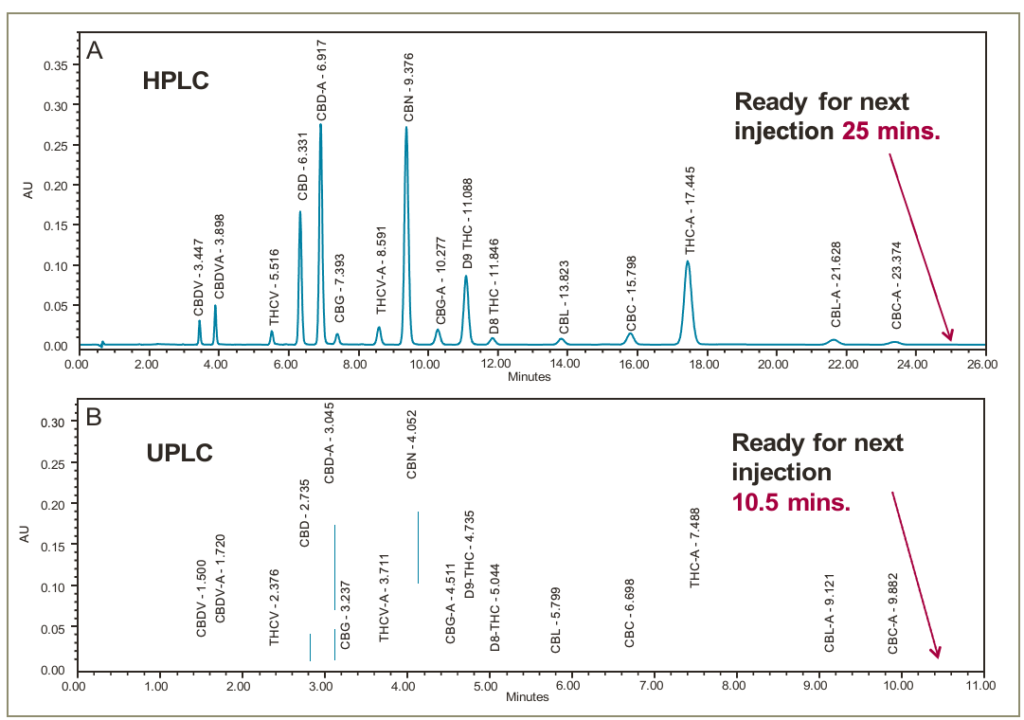
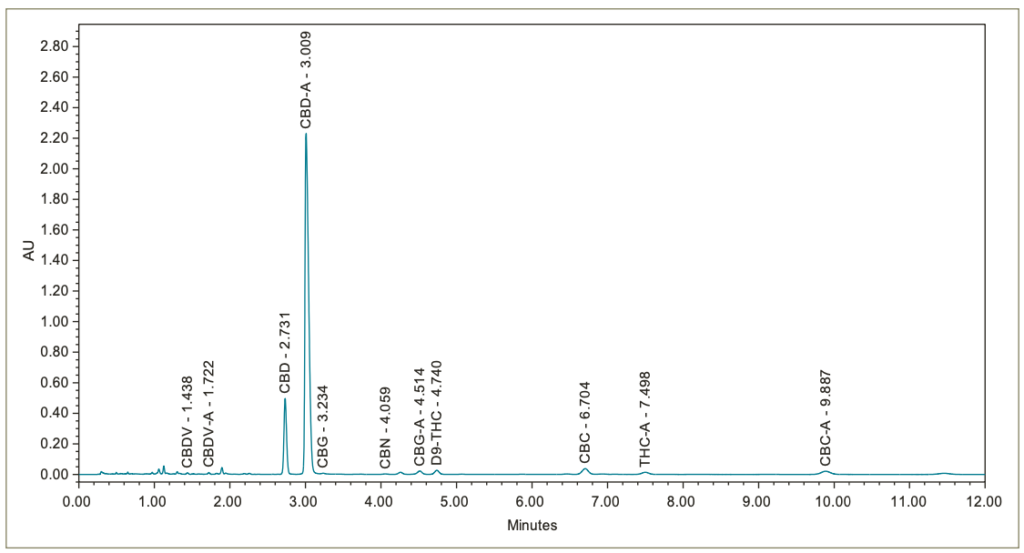
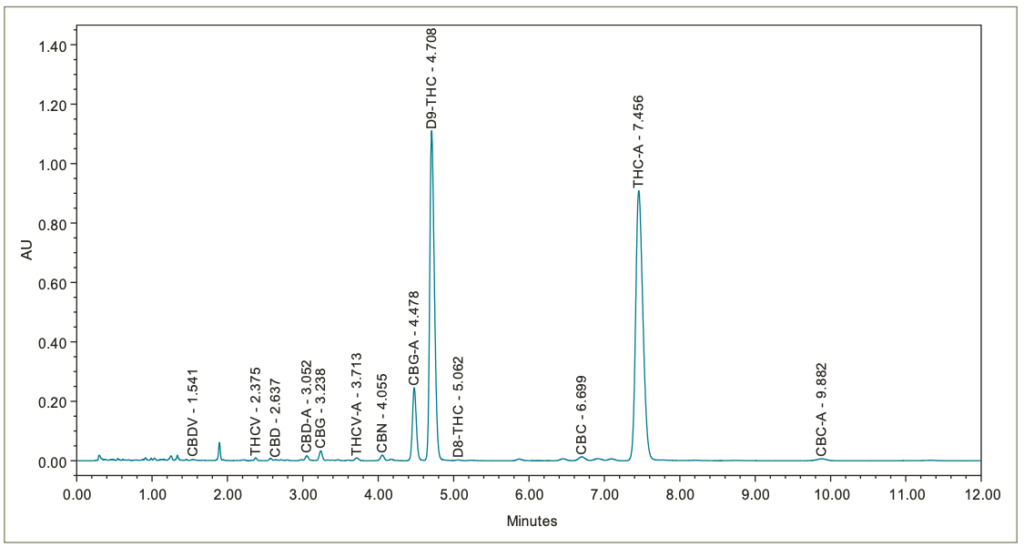
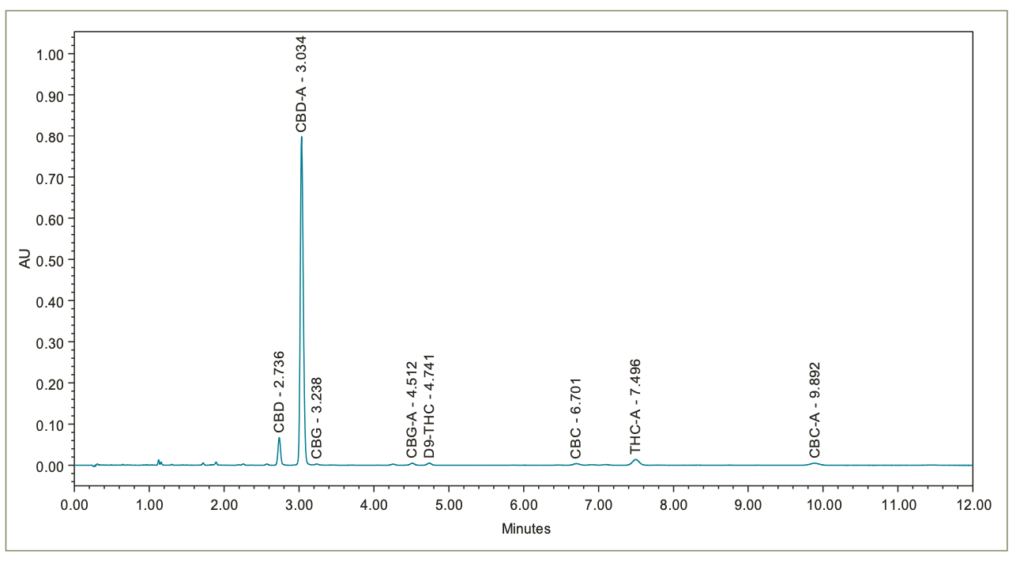
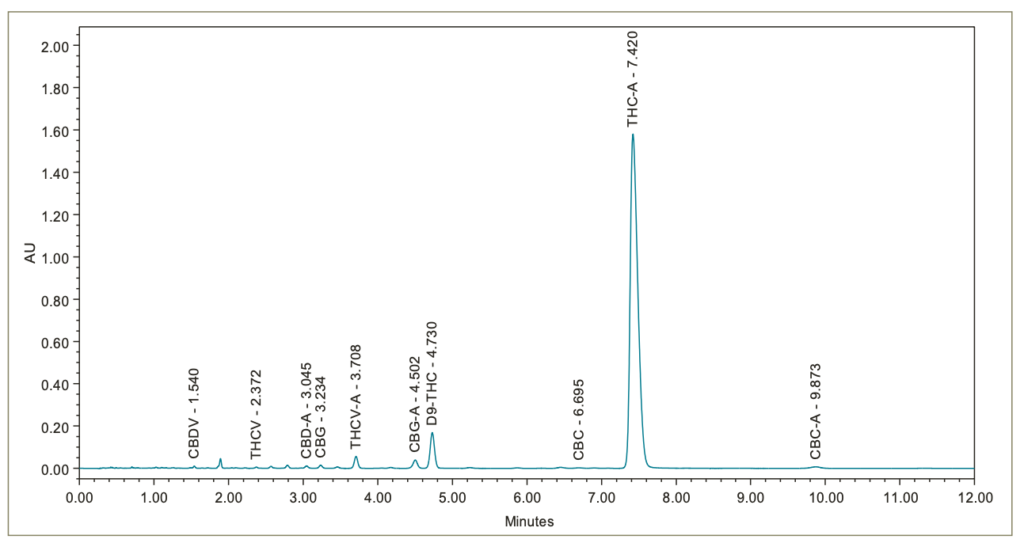
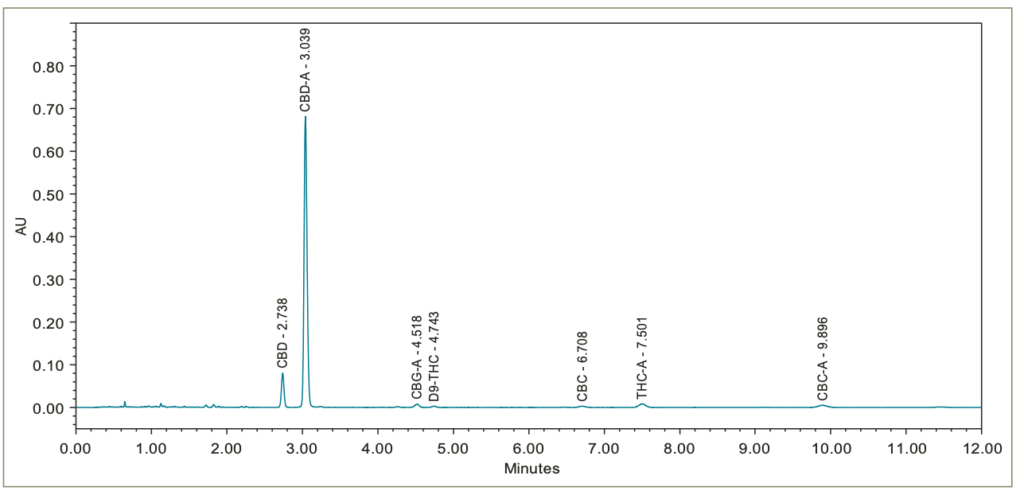
En las figuras 4, 5, 6, 7 y 8 se presentan los cromatogramas de las muestras de flores y concentrados. Los cannabinoides mayores y menores, identificados por la inyección de las soluciones estándar de referencia de cannabinoides, están etiquetados como corresponde.
La separación de cannabinoides utilizando condiciones de UPLC, en combinación con el sistema ACQUITY UPLC H-Class, proporciona un 2,5 veces el número de muestras analizadas por día, además de un ahorro del 85% en el uso de eluyentes en comparación con la HPLC (Tabla 2). De forma análoga al método HPLC, la separación emplea la columna CORTECS UPLC Shield RP18 en condiciones isocráticas para reducir aún más el tiempo del ciclo de inyección. Con el consiguiente aumento de la productividad proporcionado por la conversión a UPLC, el método descrito puede emplearse para la separación de muestras complejas de flores y concentrados que contengan cannabinoides mayores y menores con un tiempo de respuesta rápido.
| Parámetro | HPLC | UPLC | UPLC ahorro |
| Eluente usado | 52 mL | 7.2 mL | 86% |
| tiempo de corrida | 26 min | 10.3 min | 60% |
| volúmen de muestra | 5 µL | 0.7 µL | 87% |
tiempo de ciclo,
volumen de muestra e inyecciones por 24 horas.
CONCLUSIONES
■■ El sistema ACQUITY UPLC H-Class combinado con la química de partículas CORTECS UPLC Shield RP18 puede utilizarse para proporcionar una separación isocrática por UPLC de 16 cannabinoides en un tiempo de ciclo de 10,5 minutos.
■■ Se observó un aumento de 2,5 veces en el rendimiento de las muestras y un ahorro de disolventes del 86% en la separación por UPLC en comparación con la HPLC.
■■ El CBD y el (-)Δ9 -THC en 10 niveles de concentración demostraron linealidad con valores R2 ≥0,999, y la separación de 16 cannabinoides cumplió los criterios de resolución recomendados por la USP de >2 para una cuantificación precisa.
Las condiciones de UPLC demostradas son ventajosas para los laboratorios que requieren tiempos de entrega rápidos para el análisis de cannabinoides, muestras de flores y concentrados que contienen mezclas complejas de cannabinoides.
Si deseas aumentar la capacidad y eficiencia de tus procesos cromatográficos, conocer más acerca de ésta y otras alternativas en análisis de cannabinoides, por favor déjanos un mensaje en nuestro botón de contacto.
Referencias
- AJ Aubin, CE Layton. “Separation of 16 Cannabinoids in Cannabis Flower and Extracts Using a Reversed Phase Isocratic HPLC Method”, Waters Application Note, 720006426EN. (2018).
- MM Radwan, AS Wanas CS., M.A ElSohly. Natural Cannabinoids of Cannabis and Methods of Analysis. In: Chandra S., Lata H., ElSohly M. (eds) Cannabis sativa L. – Botany and Biotechnology. Springer, Cham (2017).
- CE Layton & AJ Aubin. Method Validation for Assay Determination of Cannabidiol Isolates. Journal of Liquid Chromatography & Related Technologies, Volume 41, 2018 – Issue 3 (2018).
- CE Layton and AJ Aubin. “Setting the Standard: Considerations When Handling Cannabinoid Reference Standard Preparations Used for Potency Determination.” Cannabis Science and Technology. Sept/Oct, Volume 1 – No 3 (2018).
- “System Suitability”, First supplement to USP
40-NF 35, Physical Tests/<621> Chromatography, pages 10–11. https://hmc.usp.org/sites/default/ files/documents/HMC/GCs-Pdfs/c621_1SUSP40. pdf. Accessed 2019.
- CE Layton “Beginners Guide to Preparative Liquid Chromatography”. Page 29. Waters (715005428), Library of Congress number 2017933626 (2017).
- Review Guidance, Validation of Chromatographic Methods, Center for Drug Evaluation and Research, US Food and Drug Administration (1994).