Una herramienta accesible para la identificación cualitativa de sustancias en laboratorios forenses
El detector ACQUITY QDa: una herramienta accesible para la identificación cualitativa de sustancias en laboratorios forenses
Evaluación del potencial del detector ACQUITY QDa para su uso en laboratorios de química forense y control de medicamentos
Basado en: Goshawk J., Lee R., Wood M. — Waters Corporation, 2017 · Para uso en toxicología forense
¿Por qué importa identificar sustancias con precisión?
En laboratorios de química forense y control de medicamentos, identificar con certeza qué sustancias están presentes en una muestra no es solo una cuestión técnica — tiene implicaciones legales, de salud pública y de seguridad ciudadana. Desde verificar que un medicamento contiene lo que dice en la etiqueta, hasta determinar si una sustancia incautada es ilegal, la precisión analítica lo es todo.
Técnicas tradicionales como la cromatografía de gases acoplada a espectrometría de masas (GC-MS) han sido el estándar de referencia durante décadas. Sin embargo, no son adecuadas para todos los compuestos — especialmente aquellos que son termolábiles o no volátiles.
La combinación de cromatografía líquida de ultra alta presión (UPLC) con detección por espectrometría de masas (LC-MS) ofrece una alternativa más versátil, sensible y selectiva. Y dentro de ese universo, el detector ACQUITY QDa de Waters representa un salto importante: la potencia de la detección por masas, con la simplicidad de un detector convencional.
El ACQUITY QDa fue introducido por Waters Corporation en 2013 y ha demostrado ser aplicable tanto a la identificación de medicamentos como de drogas ilícitas.
¿Qué es el match factor y cómo se interpreta?
Cuando el sistema analiza una muestra, compara el espectro de masas obtenido con los espectros almacenados en una biblioteca espectral — una especie de “base de datos de huellas moleculares”. El grado de similitud entre el espectro adquirido y el de la biblioteca se expresa como el match factor (factor de coincidencia).

El software ChromaLynx (módulo de MassLynx de Waters) automatiza este proceso: detecta picos cromatográficos, deconstruye los espectros de masa y los compara automáticamente con la biblioteca de más de 1.200 compuestos, entregando un resultado con su match factor promedio. El usuario puede incluso expandir esa biblioteca añadiendo espectros de nuevas sustancias.
Sistema cromatográfico y condiciones analíticas
El análisis se realizó utilizando el sistema ACQUITY UPLC I-Class acoplado al detector de masas ACQUITY QDa de Waters Corporation.

Sistema ACQUITY UPLC I-Class con detector QDa (Waters Corp.)
El diseño compacto del QDa permite integrarlo directamente en el stack del cromatógrafo. No requiere ajustes específicos por muestra — simplemente se enciende y funciona, como un detector óptico convencional, pero con la información adicional de la masa molecular.
| Parámetro | Condición |
| Sistema cromatográfico | ACQUITY UPLC I-Class (Waters) |
| Columna | ACQUITY UPLC BEH C18, 1.7 µm, 2.1 × 100 mm |
| Fase móvil A | Agua + 0.1% ácido fórmico |
| Fase móvil B | Acetonitrilo + 0.1% ácido fórmico |
| Modo de ionización | Electrospray positivo (ESI+) |
| Voltajes de cono | 10 V, 20 V, 35 V, 45 V y 55 V (adquisición multifunción) |
| Rango de masas | m/z 50 – 1,250 |
| Software de procesamiento | ChromaLynx Application Manager (MassLynx) |
Tabla 1. Resumen de las condiciones analíticas del método cromatográfico y de detección por masas.
Preparación de muestra y materiales
En una primera etapa, se realizaron pruebas espectrales preliminares con ocho mezclas de materiales de referencia certificados (Sigma-Aldrich). Estas mezclas se prepararon a partir de estándares certificados para garantizar la trazabilidad de los resultados.
En una segunda etapa, se prepararon muestras auténticas a partir de una selección de ocho medicamentos de venta libre:
Las tabletas/cápsulas individuales o 250 µL de los medicamentos suministrados en forma líquida se añadieron a 25 mL de una mezcla de metanol y agua (70:30) y se sometieron a ultrasonido a temperatura ambiente durante 30 minutos. Un mililitro de la solución resultante se transfirió a un tubo de microcentrífuga de 2 mL y se centrifugó a 13000 rpm durante 5 minutos. Cincuenta microlitros del sobrenadante se diluyeron con 950 µL de agua en un vial de recuperación máxima y se mezclaron mediante vórtex. El análisis LC-MS se realizó utilizando 10 µL de la solución resultante.
Resultados y discusión
Identificación exitosa en la mayoría de los medicamentos analizados
La aplicación del método cromatográfico establecido junto con la pantalla cualitativa del ChromaLynx demostró una muy buena concordancia entre los espectros de la biblioteca y los datos adquiridos, lo que permitió identificar los ingredientes activos en los medicamentos analizados.
Los resultados son destacables: en siete de los ocho medicamentos se obtuvo una identificación positiva directa contra la biblioteca existente, con match factors que en varios casos superan 880, lo que indica una coincidencia espectral excelente. El medicamento con mejor desempeño fue Buscopan® (escopolamina butilbromida), alcanzando un match factor de 902.
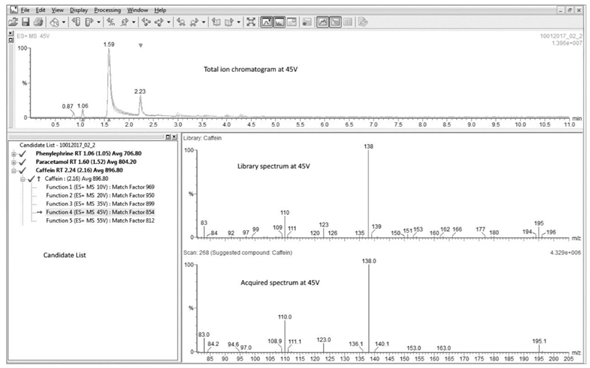
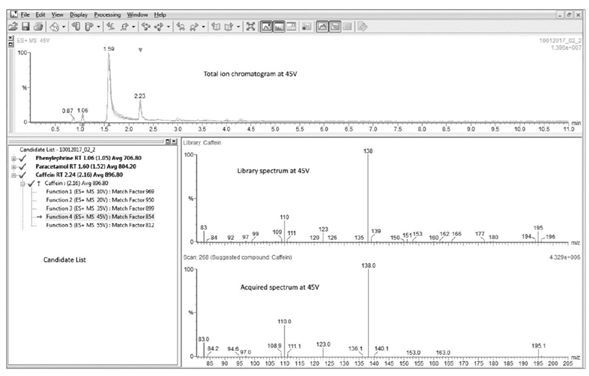
Figura 2. Pantalla del navegador ChromaLynx mostrando los resultados del análisis de LEMSIP Max Cold and Flu Remedy, destacando la identificación de cafeína con ion precursor m/z 195.
| Medicamento | Ingrediente(s) activo(s) detectado(s) | Match factor |
| LEMSIP® Max Cold and Flu | Fenilefrina 6.1 mg, paracetamol 500 mg, cafeína 25 mg | 707 / 804 / 897 |
| Galpharm™ Hayfever and Allergy | Cetirizina 10 mg | 832 |
| Entrolax® | Bisacodilo 5 mg | 889 |
| Galpharm Extra Power Pain Relief | Paracetamol 200 mg, cafeína 45 mg | 816 / 880 |
| Buscopan® | Escopolamina butilbromida 10 mg | 902 |
| Prozac® | Fluoxetina 20 mg | 883 |
| Benylin® | Guaifenesina 100 mg/5 mL | 701 |
| Imuran® | Azatioprina 50 mg | Nueva entrada ★ |
Tabla 2. Ingredientes activos identificados en cada medicamento con su match factor promedio según ChromaLynx. ★ La azatioprina no estaba en la biblioteca original; los espectros adquiridos se usaron para crear una nueva entrada en el software.
Un caso especialmente interesante fue el de Imuran® (azatioprina): no existía una entrada para este compuesto en la biblioteca de toxicología. Sin embargo, el sistema registró una respuesta de señal muy intensa y consistente en el tiempo de retención esperado para los cinco voltajes de cono analizados, lo que orientó al analista a identificar el compuesto por sus datos espectrales y crear una nueva entrada en la biblioteca. Este es uno de los grandes diferenciadores del sistema: la biblioteca puede expandirse con datos propios.
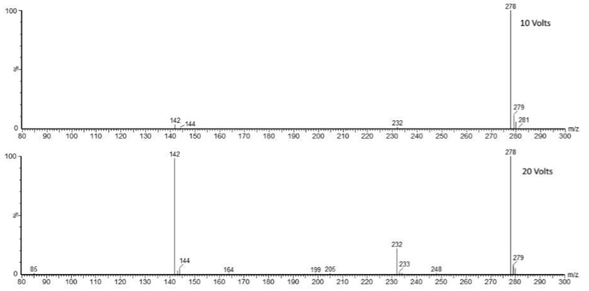
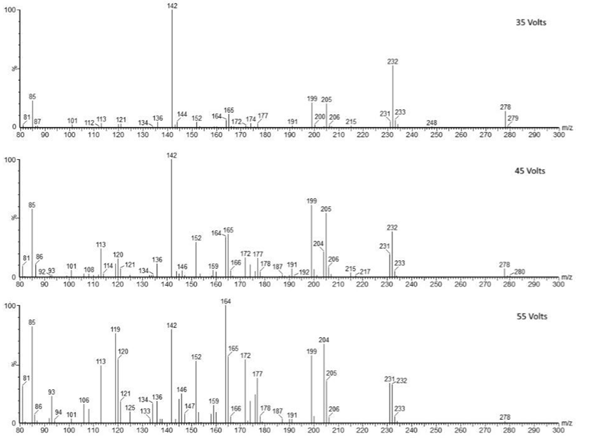
Figura 1. Espectros ESI+ de azatioprina (masa precursora m/z 278) en el ACQUITY QDa a voltajes de cono de 10 V, 20 V, 35 V, 45 V y 55 V. La fragmentación progresiva con el voltaje permite construir una firma espectral característica.
La estrategia de adquirir datos a múltiples voltajes de cono — generando diferentes grados de fragmentación molecular — es clave para construir espectros ricos en información que permitan comparaciones confiables con la biblioteca. A mayor voltaje, mayor fragmentación del ion precursor, revelando iones producto que son característicos de la estructura molecular del compuesto.
El QDa como solución de bajo costo para el control forense y de medicamentos
Los resultados de este estudio demuestran de manera convincente que el detector ACQUITY QDa, combinado con el método cromatográfico de toxicología existente de Waters y el software ChromaLynx, constituye una alternativa sólida y asequible para laboratorios que necesitan capacidades de identificación por masas sin la complejidad operativa ni el costo de los espectrómetros de masas de alta gama.
La posibilidad de reutilizar una biblioteca espectral ya establecida — con más de 1.200 compuestos — y de expandirla con datos generados en el propio laboratorio, convierte al sistema en una herramienta escalable y adaptable. Esto es especialmente valioso ante la aparición constante de nuevas sustancias psicoactivas y drogas de diseño, donde la velocidad de incorporación al protocolo de detección marca la diferencia.
Puntos clave
Match factors de hasta 902 confirman una excelente concordancia espectral entre los datos adquiridos y la biblioteca de referencia.
El sistema identificó correctamente los ingredientes activos en 7 de 8 medicamentos evaluados; el octavo permitió crear una nueva entrada en la biblioteca.
El QDa opera con la simplicidad de un detector óptico convencional — no requiere ajustes por muestra ni experticia avanzada en MS.
Representa una solución de bajo costo frente a LC-MS/MS de alta gama, con capacidad tanto cualitativa como cuantitativa en el mismo sistema.
Compatible con la biblioteca de toxicología Waters existente (>1,200 compuestos), expandible con datos propios del laboratorio.
En un entorno donde los laboratorios forenses y de control de calidad enfrentan presión constante por procesar más muestras con menos recursos, el ACQUITY QDa demuestra que la detección por masas no tiene que ser sinónimo de complejidad ni de presupuestos imposibles.
Fuente:
Goshawk J., Lee R., Wood M. Evaluation of the Potential of the ACQUITY QDa Mass Detector for Use in Forensic Chemistry and Drug Control Laboratories. Waters Technology Brief 720006004EN. Waters Corporation, 2017. Para uso en toxicología forense solamente.